نسخه چاپی
نسخه چاپی - تاریخ درج خبر:1401/07/08-١١:٥٦
بسته خبری علم و فناوری
دارویی برای درمان علائم اصلی اوتیسم/ کلید زندگی طولانی تر با یک پروتئین
ابوالفضل امیری

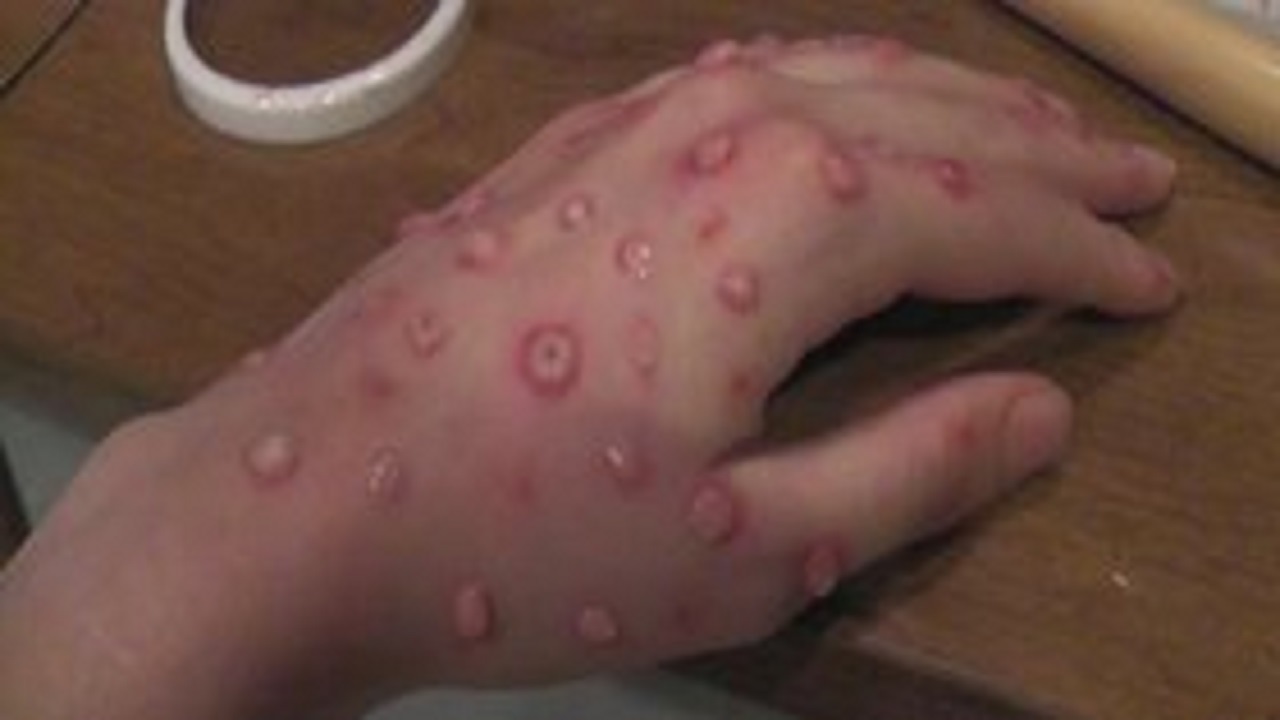
آبادان نیوز : نتایج پژوهش جدید پژوهشگران دانشگاه اسلو نشان میدهد، داروهای ضد اسهال ممکن است به درمان علائم اصلی اوتیسم کمک کند.
وراثت پذیری بالا و ناهمگونی بالینی، اختلال طیف اوتیسم (ASD) را توصیف میکنند. مشکلات ارتباط اجتماعی علائم اصلی اولیه هستند. هیچ دارویی برای درمان این علائم تایید نشده است و داروهایی که برای درمان علائم عمومی استفاده میشوند دارای عوارض جانبی مضر هستند.
پژوهشگران دانشگاه اسلو نروژ در یک مطالعه جدید به بررسی این موضوع پرداختند که آیا یک داروی موجود درمان جدیدی را ارائه میدهد یا خیر. در این مطالعه، دانشمندان با استفاده از یک مدل رایانهای حاوی پروتئینهای دخیل در اختلال طیف اوتیسم، چگونگی تاثیر داروهای مختلف بر پروتئینهای این سیستم را شناسایی کردند. آنها همچنین داروهای کاربردی برای درمان این اختلال را شناسایی کردند.
چنین شبکههایی، پروتئینها و تعاملات پیچیده بین آنها را بررسی میکند. توجه به این پیچیدگی هنگام مطالعه سیستمهای بیولوژیکی ضروری است، زیرا تأثیرگذاری بر یک پروتئین اغلب میتواند اثرات ثانویهای در جای دیگر داشته باشد.
با بررسی داروهای موجود و تعامل آنها با پروتئینها در این شبکه، پژوهشگران چندین دارو را که با فرآیند بیولوژیکی زمینهساز اختلال طیف اوتیسم مقابله میکند، شناسایی کردند.
یک داروی رایج ضد اسهال به نام لوپرامید (Loperamide) یک کاندیدای امیدوارکننده بود. دانشمندان فرضیه جالبی در مورد نحوه عملکرد آن در درمان علائم اختلال طیف اوتیسم دارند. پروتئین گیرنده مواد افیونی که اغلب تحت تاثیر داروهای مخدر مانند مورفین قرار میگیرد، به لوپرامید متصل شده و توسط آن فعال میشود. این گیرنده علاوه بر اثراتی مانند کاهش درد، بر رفتار اجتماعی نیز تأثیر میگذارد.
در مطالعات قبلی، موشهای اصلاح شده از لحاظ ژنتیکی که فاقد گیرنده μ-افیونی بودند، نقایص اجتماعی مشابه آنچه در اختلال طیف اوتیسم مشاهده میشد نشان دادند. جالب توجه است که داروهایی که گیرنده μ-افیونی را فعال میکنند به بازیابی رفتارهای اجتماعی کمک میکنند.
این یافتهها در موشها این احتمال را افزایش میدهد که لوپرامید یا سایر داروهایی که گیرنده مواد افیونی را هدف قرار میدهند، ممکن است یک استراتژی جدید برای درمان علائم اجتماعی مرتبط با اختلال طیف اوتیسم ارائه دهند. با این حال، تحقیقات بیشتری برای تأیید این نظریه مورد نیاز است.
دانشمندان میگویند یک پروتئین موسوم به CHIP میتواند سیگنال های طولانی مدت مانند گیرنده های انسولین در سلول را به تنهایی بهتر از حالت جفتی کنترل کند و میتواند کلید زندگی طولانیتر باشد.
به گفته محققان دانشگاه کلن(Cologne)، یک پروتئین به شکل واحد در مقایسه با حالت گروهی، میتواند به طور موثرتری سیگنالهای پیری را تنظیم و تعدیل کند.
این محققان در مطالعه جدید خود کشف کردهاند که پروتئینی موسوم به CHIP میتواند سیگنالهای زندگی طولانیمدت مانند گیرندههای انسولین را در سلول به تنهایی بهتر از حالت جفتی کنترل کند.
پروتئین CHIP در موقعیتهای استرس سلولی اغلب به عنوان یک "همودایمر" - اتصال دو پروتئین یکسان - دیده میشود. عملکرد اصلی آن از بین بردن پروتئینهای آسیب دیده و نادرست چین خورده است. در واقع CHIP، سلول را از این طریق تسویه میکند.
برای انجام این کار، CHIP با پروتئینهای کمکی کار میکند تا پروتئینهای اشتباه تا شده را با زنجیرههای پروتئین کوچک یوبیکوتین متصل کند.
در نتیجه، سلول، پروتئینهای آسیب دیده را شناسایی و حذف میکند. علاوه بر این، CHIP انتقال سیگنال گیرنده انسولین را تنظیم میکند.
یوبیکوتین(Ubiquitin) یک پروتئین تنظیمی کوچک است که تقریبا در تمامی بافتهای موجودات یوکاریوتی یافت میشود. این پروتئین اولین بار در سال ۱۹۷۵ میلادی کشف شد و بعدها ویژگیها و مشخصاتش در طی دهههای ۷۰ و ۸۰ میلادی مشخص شد. چهار ژن در بدن انسان موسوم به UBB ،UBC ،UBA52 و RPS27A یوبیکوتین تولید میکنند.
محققان میگویند محصولات ژنی افزایش دهنده عمر نمیتوانند فعال شوند، زیرا CHIP به گیرنده متصل شده و آن را تجزیه میکند.
تیم تحقیقاتی به سرپرستی پروفسور "تورستن هاپ" اکنون نشان داده است که CHIP ممکن است خود را با یوبیکوتین یکی کند و از تشکیل دایمر(حالت جفتی) جلوگیری کند. آنها همچنین از سلولهای انسانی و یک نماتد موسوم به "Caenorhabditis elegans" در این آزمایش استفاده کردند.
"ویشنو بالاجی" نویسنده ارشد این مطالعه گفت: اینکه CHIP به تنهایی یا به صورت جفت کار کند، به وضعیت سلول بستگی دارد. تحت استرس، پروتئینهای نادرست تا شده و همچنین پروتئینهای کمکی زیادی وجود دارد که به CHIP متصل میشوند و از یوبیکوتین شدن خودکار، خود برچسبگذاری با یوبیکوتین جلوگیری میکنند.
وی افزود: پس از اینکه CHIP با موفقیت پروتئینهای معیوب را پاکسازی کرد، میتواند پروتئینهای کمکی را نیز برای تجزیه علامتگذاری کند. این به CHIP اجازه میدهد تا خود را در همه جا بیان کند و دوباره به عنوان یک مونومر عمل کند.
"تورستن هاپ" میگوید: جالب است که تعادل مونومر-دایمر CHIP در بیماریهای عصبی مختل شده است.
گام بعدی این است که محققان تعیین کنند آیا پروتئین یا گیرنده دیگری وجود دارد که مونومر CHIP با آنها تعامل داشته باشد و عملکرد آنها را کنترل کند؟
محققان به منظور ایجاد درمانهای تخصصیتر در آینده، به طور ویژه کنجکاو هستند که کدام بافتها، اندامها و بیماریها دارای غلظت بالاتری از مونومرها یا دایمرهای CHIP هستند.
نتایج این مطالعه در مجله Molecular Cell منتشر شده است.
| نام : | |
| ایمیل : | |
| *نظرات : | |
| | |
| متن تصویر: | |